Grafitas, molekulinė formulė: C, molekulinė masė: 12,01, yra elemento anglies forma, kiekvienas anglies atomas yra sujungtas trimis kitais anglies atomais (išdėstytais korio šešiakampiuose), kad susidarytų kovalentinė molekulė. Kadangi kiekvienas anglies atomas išskiria elektronus, tuos, kurie gali laisvai judėti, todėl grafitas yra laidininkas.
Grafitas yra vienas minkštiausių mineralų, o jo naudojimas apima pieštukų laidus ir tepalus. Anglis yra nemetalinis elementas, esantis periodinės lentelės antrojo ciklo IVA grupėje. Grafitas susidaro aukštoje temperatūroje.
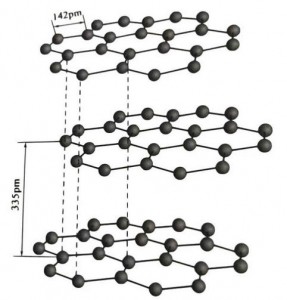
Grafitas yra kristalinis anglies elementų mineralas, o jo kristalinė gardelė yra šešiakampė sluoksniuota struktūra. Atstumas tarp kiekvieno tinklelio sluoksnio yra 3,35 A, o anglies atomų atstumas tame pačiame tinklelio sluoksnyje yra 1,42 A. Tai šešiakampė kristalų sistema su visišku sluoksniuotu skilimu. Skilimo paviršių daugiausia sudaro molekuliniai ryšiai, mažiau patrauklūs molekulėms, todėl jo natūrali plūdė yra labai gera.
Grafito kristaluose anglies atomai tame pačiame sluoksnyje sudaro kovalentinį ryšį su sp2 hibridizacija, o kiekvienas anglies atomas yra sujungtas su trimis kitais atomais trimis kovalentiniais ryšiais. Šeši anglies atomai sudaro šešių ištisinį žiedą toje pačioje plokštumoje, besitęsiantį į lamelės struktūrą, kur CC jungties jungties ilgis yra 142 pm, o tai yra tiksliai atominio kristalo jungties ilgio diapazone, taigi tam pačiam sluoksniui , tai atominis kristalas. Anglies atomai toje pačioje plokštumoje turi vieną p orbitą, kurios persidengia viena su kita. Elektronai yra santykinai laisvi, prilygsta laisviesiems elektronams metaluose, todėl grafitas gali laiduoti šilumą ir elektrą, kas būdinga metalo kristalams. Taigi taip pat klasifikuojami kaip metaliniai kristalai.
Vidurinį grafito kristalo sluoksnį skiria 335 pm, o atstumas yra didelis. Jis derinamas su van der Waals jėga, tai yra, sluoksnis priklauso molekuliniam kristalui. Tačiau kadangi anglies atomų surišimas tame pačiame plokščiame sluoksnyje yra labai stiprus ir itin sunkiai sunaikinamas, grafito tirpimo taškas taip pat yra labai aukštas, o jo cheminės savybės stabilios.
Atsižvelgiant į specialų sujungimo būdą, grafitas negali būti laikomas monokristalu ar polikristalais, dabar paprastai laikomas mišriu kristalu.
Paskelbimo laikas: 2023-07-31